Luigi Ricciardi 1 , Rosa Mazzeo 2,*© , Angelo Raffaele Marcotrigiano 1 , Guglielmo Rainaldi 3 , Paolo Iovieno 4 , Vito Zonno 1 , Stefano Pavan 1© și Concetta Lotti 2,*
- 1 Departamentul de științe ale solului, plantelor și alimentelor, Unitatea de genetică și ameliorare a plantelor Universitatea din Bari, Via Amendola 165/A, 70125 Bari, Italia; luigi.ricciardi@uniba.it (LR);angelo.marcotrigiano@uniba.it (BRAŢ); vito.zonno@uniba.it (VZ); stefano.pavan@uniba.it (SP)
- 2 Departamentul de Științe ale Agriculturii, Alimentației și Mediului, Universitatea din Foggia, Via Napoli 25, 71122 Foggia, Italia
- 3 Departamentul de Bioștiințe, Biotehnologii și Biofarmaceutice, Universitatea din Bari, Via Orabona 4, 70125 Bari, Italia; guglielmo.rainaldi@uniba.it
- 4 Departamentul Tehnologii Energetice, Divizia Bioenergie, Biorafinărie și Chimie Verde, Centrul de Cercetare ENEA Trisaia, SS 106 Ionica, km 419+500, 75026 Rotondella (MT), Italia; paolo.iovieno@enea.it
* Corespondenţă: rosa.mazzeo@unifg.it (RM); concetta.lotti@unifg.it (CL)
Rezumat:
Ceapă (Allium cepa L.) este a doua cea mai importantă cultură de legume la nivel mondial și este larg apreciată pentru beneficiile sale pentru sănătate. În ciuda importanței sale economice semnificative și a valorii sale ca aliment funcțional, ceapa a fost slab investigată în ceea ce privește diversitatea sa genetică. Aici, am analizat variația genetică a „ceapă roșie Acquaviva” (ARO), o rasă locală cu o istorie veche de un secol de cultivare într-un mic oraș din provincia Bari (Apulia, sudul Italiei). Un set de 11 markeri de microsateliți au fost utilizați pentru a explora variația genetică într-o colecție de germoplasmă constând din 13 populații ARO și trei tipuri comerciale comune. Analizele structurii genetice cu metode parametrice și neparametrice au evidențiat că ARO reprezintă un bazin genetic bine definit, clar distinct de rasele locale Tropea și Montoro cu care este adesea greșit. Pentru a oferi o descriere a bulbilor, utilizați în mod obișnuit pentru consumul proaspăt, s-au evaluat conținutul de solide solubile și piezitatea, prezentând o dulceață mai mare în ARO față de cele două rase locale menționate mai sus. În ansamblu, prezentul studiu este util pentru viitoarea valorificare a ARO, care ar putea fi promovată prin etichete de calitate care ar putea contribui la limitarea fraudelor comerciale și la îmbunătățirea veniturilor micilor fermieri.
Introducere
Genul Allium cuprinde aproximativ 750 de specii [1], dintre care ceapa (Allium cepa L., 2n = 2x =16) este una dintre cele mai răspândite. A. cepa are un ciclu bienal și un comportament reproductiv de încrucișare. În prezent, producția globală de ceapă (97.9 Mt) o face a doua cea mai importantă cultură de legume după tomate [2]. Din cele mai vechi timpuri, bulbii de ceapă au fost folosiți atât ca hrană, cât și în aplicații medicinale populare. Într-adevăr, egiptenii antici au raportat deja câteva formule terapeutice bazate pe utilizarea usturoiului și a cepei într-un papirus medical din 1550 î.Hr., Codex Ebers [3].
Această legumă versatilă și sănătoasă este consumată crudă, proaspătă sau ca produs procesat și folosită pentru a spori gustul multor feluri de mâncare. Mai multe studii recente susțin că consumul de ceapă poate reduce riscul de boli cardiovasculare [4,5], obezitate [6], diabet [7] și diferite forme de cancer [8–10]. Proprietățile de sănătate a cepei sunt adesea atribuite nivelurilor ridicate de două clase de compuși nutraceutici: flavonoide și sulfoxizi de alk(en)il cisteină (ACSO). Prima clasă include flavonoli și antociani. Quercetina este principalul flavonol detectabil, cunoscut pentru proprietățile sale puternice antioxidante și antiinflamatorii în captarea radicalilor liberi și legarea ionilor metalelor tranziționale. [11]; în timp ce antocianinele conferă culoare roșie/violet unor soiuri de ceapă. În ceea ce privește ACSO, cea mai abundentă este izoaliina [(+)-trans-S-1-propenil-L-cisteină sulfoxid] [12], un aminoacid sulfuros nevolatil și neproteinogen stocat în celule, care este indirect responsabil pentru aroma și gustul înțepător al cepei [13]. La distrugerea țesutului, izoaliina este scindată de enzima aliinaza pentru a produce o serie de compuși volatili (piruvat, amoniac, tiosulfonați și S-oxid de propanetial) care induc ruperea și provoacă miros neplăcut (pungență). [14]. Pungența cepei este adesea măsurată ca cantitatea, per gram de greutate proaspătă, de acid piruvic generat prin hidroliză. [15,16].
În țările din bazinul mediteranean, propus ca unul dintre centrele secundare de diversitate ale a. tulpina [17,18], bulbii de ceapă prezintă o mare variabilitate în formă, dimensiune, culoare, substanță uscată și picătură [19-unu]. În plus, fertilizarea pe bază de sulf, practicile agronomice, tipul de sol, condițiile climatice și genotipul soiurilor sau raselor locale pot influența calitatea bulbilor prin conferirea unor valori organoleptice și nutritive deosebite. [23-unu]. În Italia, în ciuda disponibilității largi de germoplasmă de ceapă, doar câteva soiuri de ceapă sunt adesea supuse unor studii științifice și caracterizate corespunzător. [28,29].
Caracterizarea completă genetică și fenotipică a agro-biodiversității este crucială pentru a asigura conservarea adecvată a resurselor genetice vegetale și pentru a promova utilizarea genotipurilor specifice în lanțul valoric [30-unu]. Markerii de repetare a secvenței simple (SSR) au fost adesea aleși pentru mapare [33-unu], amprentarea ADN și discriminarea soiurilor [36-unu]și estimarea fiabilă a variabilității genetice în interiorul și între rasele locale [39-unu], deoarece sunt specifice de locus, multi-alelice, moștenite codominant, foarte reproductibile și potrivite pentru genotiparea automată.
În studiul de față, ne-am concentrat atenția asupra unei rase tradiționale din Apulia, „ceapa roșie Acquaviva” (ARO), care este cultivată conform metodelor de agricultură ecologică într-o zonă mică a orașului Acquaviva delle Fonti, din provincia Bari. (Apulia, sudul Italiei). Bulbii acestei specii locale sunt mari și turtiți și de culoare roșie și sunt folosiți în mare măsură în rețetele locale. Deși ARO a câștigat marca de calitate „Prezidiul Slow Food”, producția sa ar putea fi promovată și protejată în continuare prin mărci de calitate ale Uniunii Europene, cum ar fi indicația geografică protejată (IGP) și denumirea de origine protejată (POD), deoarece acestea ar putea contribui la limitarea fraudelor comerciale și îmbunătățirea veniturilor micilor fermieri. Aici, markerii moleculari SSR au fost folosiți ca instrumente puternice pentru a evalua variația genetică între populațiile ARO și pentru a discrimina această rasă locală de alte două specii de ceapă roșie din sudul Italiei. În plus, am estimat conținutul de substanțe solide și solubile pentru a evalua aroma ARO în raport cu cererea pieței.
REZULTATE
Înființarea Colecției de Germoplasme de Ceapă Roșie Acquaviva și Caracterizare Morfologică
Semințele a 13 populații din rasa locală ARO, donate de fermieri în cadrul proiectului BiodiverSO Regiunea Apulia au fost folosite pentru a stabili o colecție de germoplasmă ARO.
Descriptori morfologici, legati de bulb, piele si carne au fost colectati pe germoplasma ARO si pe trei rase de ceapa, doua apartinand rasei locale „ceapa rosie de Tropea” (TRO) si una rasei locale „ceapa cupru Montoro” (MCO) (Figura 1). Toți becurile ARO erau plate și erau caracterizate de pielea externă roșie și carnea cu diferite nuanțe de roșu. În schimb, carnea bulbilor TRO a fost complet roșie, în timp ce carnea bulbilor MCO a fost slab pigmentată (Tabelul S1). Analiza biochimică a permis evaluarea conținutului de solid solubil și a picăturii. După cum se raportează în tabel 1, valorile medii ale conținutului solid solubil al bulbilor în populațiile ARO a fost de 7.60 și a variat de la 6.00 (ARO12) la 9.50° Brix (ARO11 și ARO13). Această valoare a fost mai mare decât cea estimată pentru rasele locale TRO și MCO (4.25, respectiv 6.00° Brix).

Tabelul 1. Conținutul de solubile solide și valorile înțepătoare evaluate în populațiile „Acquaviva Red Onion” (ARO), „Tropea Red Onion” (TRO) și „Montoro Copper Onion” (MCO) *.
| COD | Conținut solid solubil (Brix) | iuteala (pmolg-1 FW) | ||
| medie | CV y (%) | medie | CV y (%) | |
| ARO1 | 6.25 D * | 5.65 | 5.84 ab * | 23.78 |
| ARO2 | 7.25 DC | 4.87 | 6.51 | 22.98 |
| ARO3 | 7.50 BCD | 9.42 | 5.28 pop | 22.88 |
| ARO4 | 7.50 BCD | 0.00 | 6.97 | 3.74 |
| HOOP 5 | 7.50 BCD | 0.00 | 6.80 | 9.68 |
| ARO6 | 6.25 D | 5.65 | 4.51 pop | 39.18 |
| ARO7 | 7.25 DC | 4.87 | 5.25 pop | 15.44 |
| ARO8 | 9.00 AB | 0.00 | 7.04 | 3.49 |
| ARO9 | 8.25 ABC | 4.28 | 6.84 | 0.15 |
| ARO10 | 7.00 DC | 0.00 | 5.94 pop | 6.57 |
| ARO11 | A 9.50 | 7.44 | 5.54 pop | 16.43 |
| ARO12 | 6.00 D | 0.00 | 4.91 pop | 9.70 |
| ARO13 | A 9.50 | 7.44 | 6.63 | 24.93 |
| MCO | 6.00 D | 0.00 | 4.18 pop | 2.66 |
| TRO1 | E 4.25 | 8.31 | 2.80 b | 2.10 |
| TRO2 | E 4.25 | 8.31 | 4.28 pop | 4.79 |
* Mijloacele cu aceleași litere în litere mari sau mici nu sunt diferite statistic la 0.01P sau, respectiv, 0.05P (testul SNK). y Coeficient de variație.
Valoarea medie a picantității ARO, evaluată prin intermediul conținutului de acid piruvic, a fost de 6.00, a variat între 4.51 pmol g-1 FW (ARO6) până la 7.04 (ARO8). Această valoare a fost mai mare decât cea estimată în rasele locale TRO și MCO (3.54 pmol g-1 FW și 4.18 pmol g-1 FW, respectiv).
Polimorfismul SSR și relațiile genetice între accesări
În studiul de față, 11 din 37 de combinații de primeri SSR testate au furnizat polimorfisme cu un singur loc, adică, produc cel mult două produse de amplificare la un singur individ. În total, 55 de alele au fost detectate la 320 de indivizi cu un număr de alele per locus variind de la 2 (ACM147 și ACM 504) la 11 (ACM132) și o valoare medie de 5 alele (Tabelul). 2). În populațiile individuale, numărul de alele (Na) a variat de la 1.94 (ACM147 și ACM504) la 5.38 (ACM132), în timp ce numărul efectiv de alele (Ne) a variat de la 1.41 (ACM152) la 2.82 (ACM449). Discrepanțele între valorile Na și Ne s-au datorat prezenței alelelor cu frecvență scăzută în populații și predominării doar a câtorva alele. Cea mai mare valoare observată a heterozigozității (Ho) a fost evidențiată pentru ACM138 și ACM449 (0.62), în timp ce cea mai mică a fost asociată cu ACM152 (0.25). Heterozigositatea așteptată (He), care corespunde așteptărilor teoretice într-o populație panmictică, a variat de la 0.37 (ACM504) la 0.61 (ACM132, ACM138 și ACM449). Indicele de fixare al lui Wright (Fis), a afișat valori apropiate de zero (medie 0.05) pentru toți markerii, indicând valori similare între nivelurile de heterozigoție observate și așteptate, așa cum era de așteptat pentru o specie încrucișată. Eficiența markerului SSR individual în amprentarea genetică a fost estimată prin indicele conținutului de informații polimorfe (PIC), cu o valoare medie de 0.48 și a variat de la 0.33 (ACM504) la 0.67 (ACM132). Un alt indice de eficiență, indicele de informare al lui Shannon (I) a afișat o valoare medie de 0.84, iar valorile presupuse variau de la 0.45 (ACM152) la 1.20 (ACM132).
Tabelul 2. Caracteristicile de polimorfism ale celor 11 markeri SSR utilizați pentru a estima diversitatea genetică în populațiile ARO, TRO și MCO. Numărul total de alele (Na), intervalul de mărime a benzii și indicele conținutului de informații polimorfe (PIC) Consultați setul total de 320 de indivizi genotipați în acest studiu. Număr de alele (Na), numărul de alele eficiente (Ne), heterozigoză observată (Ho), heterozigote așteptată (He), indice de fixare (Fis), și Indicele de informații al lui Shannon (I) se referă la valori medii calculate din 16 populații, fiecare compusă din 20 de indivizi.
| Locus. | Na total | Interval de dimensiuni (bp) | PIC | medie | |||||
| Na | Ne | Ho | He | I | Fis | ||||
| ACM91 | 4 | 189-205 | 0.40 | 2.63 | 1.72 | 0.38 | 0.39 | 0.66 | 0.04 |
| ACM101 | 4 | 229-241 | 0.52 | 2.94 | 2.37 | 0.53 | 0.56 | 0.92 | 0.06 |
| ACM132 | 11 | 186-248 | 0.67 | 5.38 | 2.78 | 0.55 | 0.61 | 1.20 | 0.09 |
| ACM138 | 5 | 242-272 | 0.66 | 3.69 | 2.82 | 0.62 | 0.61 | 1.09 | -0.02 |
| ACM147 | 2 | 264-266 | 0.37 | 1.94 | 1.83 | 0.44 | 0.44 | 0.62 | -0.01 |
| ACM152 | 4 | 228-244 | 0.25 | 2.38 | 1.41 | 0.25 | 0.27 | 0.45 | 0.07 |
| ACM235 | 4 | 286-298 | 0.41 | 2.81 | 1.77 | 0.44 | 0.41 | 0.72 | -0.06 |
| ACM446 | 6 | 108-120 | 0.56 | 3.50 | 2.48 | 0.49 | 0.58 | 1.01 | 0.16 |
| ACM449 | 8 | 120-140 | 0.66 | 4.88 | 2.82 | 0.62 | 0.61 | 1.18 | -0.03 |
| ACM463 | 5 | 202-210 | 0.47 | 3.38 | 1.95 | 0.46 | 0.48 | 0.83 | 0.05 |
| ACM504 | 2 | 188-192 | 0.33 | 1.94 | 1.64 | 0.30 | 0.37 | 0.54 | 0.20 |
| medie | 5 | 0.48 | 3.22 | 2.15 | 0.46 | 0.48 | 0.84 | 0.05 |
Dintre populații, ARO3, ARO6, ARO8, ARO10, TRO1 și MCO au prezentat un nivel ridicat de variație genetică (Ho > 0.5), în timp ce cea mai scăzută diversitate a fost observată în populația ARO7 (Ho = 0.27) (Tabelul suplimentar S2). În general, toate accesările au afișat Fis valori apropiate de zero (Fis valoare medie = 0.054), așa cum era de așteptat în condiții de împerechere aleatoare.
Analiza varianței moleculare și a structurii genetice
Împărțirea ierarhică a variației genetice între și în cadrul populațiilor a fost calculată de AMOVA. Rezultatele au evidențiat o fracțiune considerabilă a variației genetice în cadrul populațiilor (87%). Variația între populații, 13%, a fost foarte semnificativă (P < 0.001) (Tabel 3). Valorile perechi ale parametrului Fpt, un analog cu indicele de fixare Fst al lui Wright, variind de la 0.002 (ARO2/ARO10) la 0.468 (ARO7/TRO2), au fost semnificative (P < 0.05), cu excepția a nouă comparații pe perechi (Tabelul suplimentar S3).
Tabelul 3. Analiza varianței moleculare a 320 de genotipuri din 16 populații de Allium cepa L.
| Sursă | df | Suma patratelor | Estimarea variației | Varianta (%) | Fpt | P |
| In randul populatiilor | 15 | 458.63 | 1.16 | 13% | ||
| In cadrul populatiilor | 304 | 2272.99 | 7.50 | 87% | 0.134 | 0.001 |
| Total | 319 | 2731.62 | 8.66 |
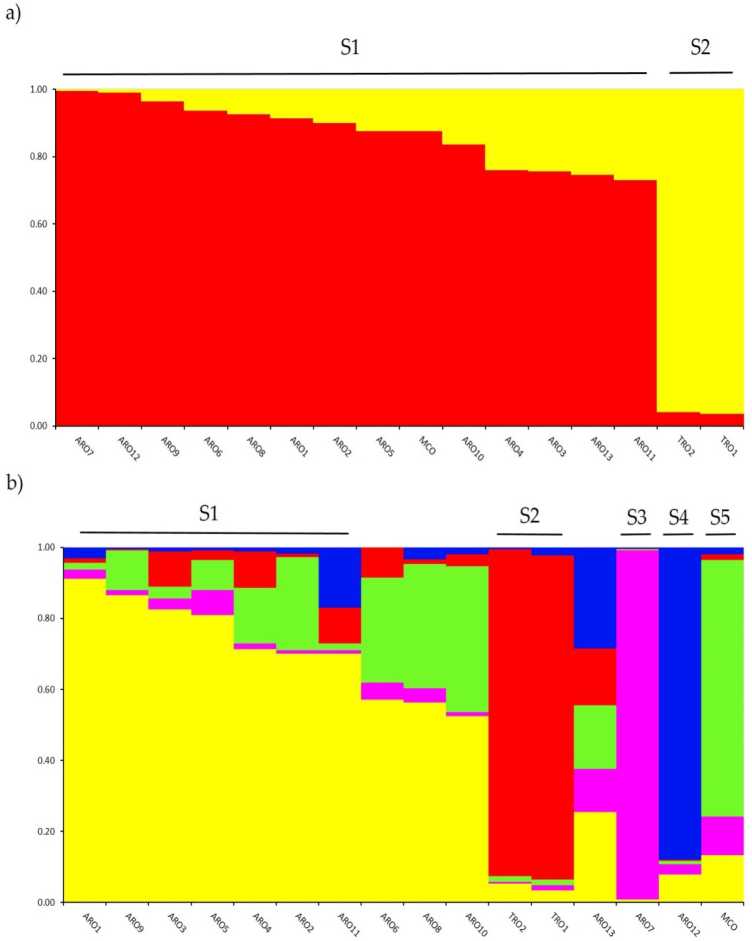
Investigarea structurii genetice în a. tulpina colecția genotipată în acest studiu a fost realizată prin intermediul analizei de clustering bazată pe model de amestec implementată în software-ul STRUCTURE. Metoda Evano AK a sugerat subdiviziunea în două grupuri (K = 2) ca fiind cea mai informativă pentru date CCD,cu the următor cel mai mare peak la K = 5 (suplementaiv Rgure S1). O pentru K = 2, ahpopulations wera funduligned de asemeneanșif cele două clustere cu un coeficient rnernbertoip (q) > 0.7. Ca shown in Figura 2a, primul cluster (numit S1) a inclus MCO și toate populațiile ARO, în timp ce clusterul S2 a grupat cele două populații TRO. La K = 5, oferind o descriere mai profundă a setului de date (Figura 2b), 75% dintre accesări au fost alocate unuia dintre cele cinci clustere. Separarea dintre ARO (S1) și TRO (S2) a fost confirmată, deși unele populații ARO au fost amestecate (q < 0.7) sau grupate separat în cele două noi grupuri S3 și S4 (ARO7 și, respectiv, ARO12). Interesant este că tipul comercial MCO a format un grup distinct (S5) separat de ceapa roșie din Apulia.
Relații genetice între populații
Polimorfismul SSR a permis trasarea unei dendrograme a diversității genetice, iar rezultatele analizei filogenetice sunt prezentate în figura 3a. Aici, colecția de germoplasmă a fost împărțită în cinci grupuri puternic susținute de valorile bootstrap. Populațiile ARO7 și ARO12 au fost imediat separate de populațiile rămase și au format două grupuri distincte. Al treilea cluster a inclus cele două populații comerciale de TRO, în timp ce al patrulea nod a împărțit MCO de unsprezece populații ARO. Relația genetică care apare între populații a fost investigată în continuare prin intermediul analizei coordonatelor principale (PCoA) (Figura 3b). După cum sa subliniat anterior, populațiile ARO au fost grupate strâns, cu excepția ARO12 și ARO7, care au apărut în poziții izolate în diagrama PCoA. Cele două populații TRO și MCO au fost împrăștiate în panoul din dreapta jos al parcelei.
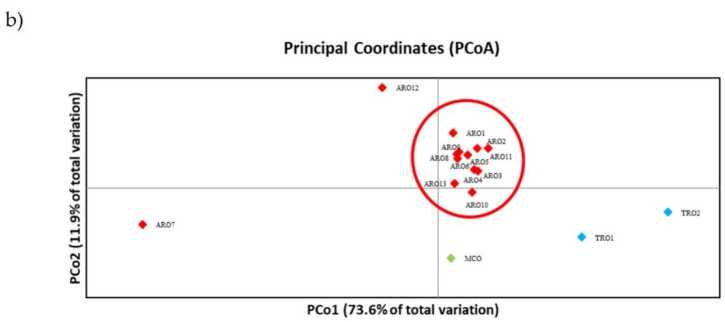
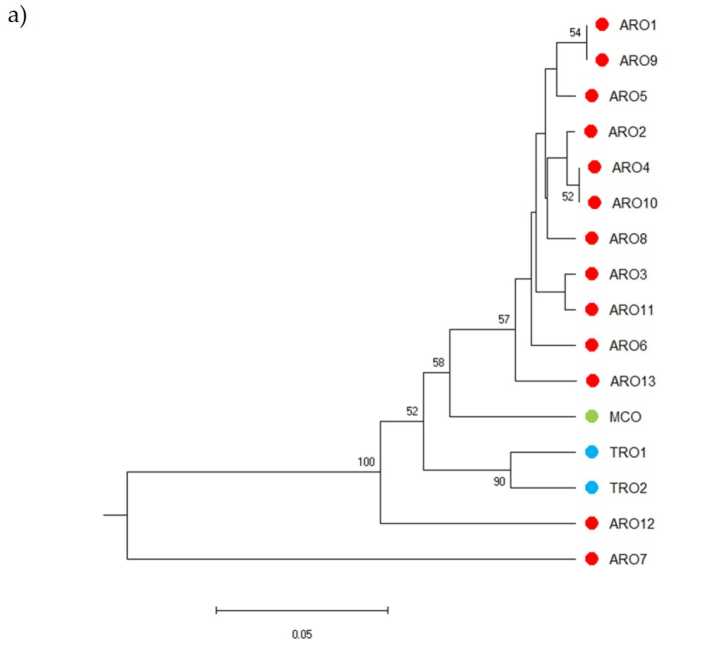
Figura 3. Diversitatea genetică între 16 a. tulpina populațiile caracterizate în acest studiu, pe baza profilului lor SSR. (a) Dendrograma UPGMA a distanței genetice. Valorile suportului bootstrap >50 sunt indicate deasupra nodurilor corespunzătoare; (b) analiza componentelor principale (PCoA). Clusterul încercuit în roșu s-a potrivit complet cu grupul generat prin analiza filogenetică și constituit din 11 accesări ARO.
Discuție
În cadrul cantității mari de agro-biodiversitate cultivată în mod tradițional în sudul Italiei, speciile locale de ceapă reprezintă produse de nișă care trebuie protejate de riscul de eroziune genetică și de amenințarea înlocuirii cu soiuri moderne. În cadrul proiectului regional BiodiverSO, care vizează colectarea, caracterizarea, promovarea și protejarea resurselor genetice din regiunea Apulia strâns legate de moștenirea locală, am înființat o colecție de semințe de 13 populații din rasa locală ARO. Am raportat prima evaluare a variației ARO în ceea ce privește polimorfismele ADN și doi parametri biochimici, conținutul de solid solubil și acid piruvic, legat de trăsăturile de aromă și de importanță pentru acceptarea produselor proaspete negătite. În plus, datele despre rasa locală ARO au fost comparate cu cele colectate pe alte două specii de ceapă pigmentată cu care se confunda adesea.
Analizele biochimice au evidențiat dulceața celor 13 populații de ARO, legată de conținutul ridicat de solide solubile și de picătură medie, conform ghidurilor industriei de ceapă dulce. [31]. Becurile ARO erau mai dulci decât cele ale raselor locale TRO și MCO și prezentau o picătură puțin mai mare. Cu toate acestea, dulceața în ceapă se datorează unui echilibru între conținutul de zahăr și picant, prin urmare această caracterizare ar putea fi utilă pentru a susține selecția genotipurilor de valoare, efectuată de obicei de fermieri doar pe baza morfologiei.
Markerii SSR au fost confirmați a fi un instrument util pentru discriminarea genotipurilor, deși colectați într-o zonă îngustă de creștere, cum ar fi orașul Acquaviva delle Fonti. Markerii selectați au afișat un număr mai mare de alele decât markerii raportați anterior [43] și [44], dar mai mici decât markerii raportați de [45]. Mai mult, 50% din setul nostru de markeri au arătat valori ale indicelui PIC mai mari de 0.5, dovedindu-se a fi potrivite pentru a discrimina populațiile din colecție, așa cum sugerează [46]. Evaluarea diversității în cadrul populațiilor a relevat valori similare între Ho și He, rezultând un Fi scăzuts valorile. Acest lucru este în acord cu natura de încrucișare a A. cepa, care suferă grav de depresie de consangvinizare [47]. Fis valoarea calculată în populațiile de ceapă luate în considerare în acest studiu (0.054) a fost mai mică decât cea raportată anterior de [45] (0.22) și aproape identică cu cea găsită de [31] (0.08) și [48] (0.00) care au evaluat diversitatea genetică la rasele locale de ceapă din nord-vestul Spaniei și, respectiv, Niger. Nivelurile remarcabile de heterozigozitate în populațiile ARO întăresc ideea că Apulia reprezintă un centru de diversitate pentru multe specii horticole. [32, 42, 49-unu].
AMOVA a subliniat că majoritatea variațiilor moleculare din colecția genotipată în acest studiu se află în cadrul populațiilor. Cu toate acestea, diferențierea genetică semnificativă între populații (FPT valori) au relevat apariţia stratificării genetice. De fapt, deși rezultatele noastre au indicat prezența uniformității genetice în majoritatea populațiilor ARO, formând un cluster bine definit, populațiile ARO7 și ARO12 au afișat un profil genetic clar distinct. Acest rezultat s-ar putea datora unei origini diferite a semințelor folosite de cei doi fermieri de la care au fost colectate populațiile. Mai mult, pe baza rezultatelor obținute, rasa locală ARO poate fi considerată clar distinctă la nivel genetic de rasele locale TRO și MCO. Într-un studiu recent, [29] a evaluat diversitatea genetică a mai multor rase de ceapă italiene, inclusiv „Acquaviva”, „Tropea” și „Montoro”. Deși autorii au folosit markeri SNP pentru a evalua diversitatea genetică a unei colecții mai largi de ceapă, genotiparea nu a fost capabilă să discrimineze „Acquaviva” de ceapa „Tropea” și „Montoro”. Probabil, această discrepanță se datorează valorii medii scăzute a PIC găsită (0.292), sugerând o informație generală modestă a loci analizați, așa cum este susținut de [29]. În plus, pentru a investiga prezența substructurii în clusterul lor italian, ar fi fost mai bine să analizăm genotipurile italiene separat de restul colecției. Probabil că ar fi permis vizualizarea unui model de diversitate genetică legat de stratificarea geografică sau de trăsături sub selecție empirică.
În concluzie, prezentul studiu reprezintă un raport cuprinzător despre o rasă de ceapă asociată cu moștenirea culturală locală și de importanță economică pentru fermieri. Rezultatele noastre evidențiază că, cu câteva excepții, ARO se caracterizează printr-un pool genetic bine definit, care merită să fie protejat de riscul de eroziune genetică. Prin urmare, constituirea unei colecții reprezentative a acestei surse valoroase de diversitate genetică a fost crucială. În cele din urmă, caracterizarea genetică și fenotipică a ARO ar putea fi utilă pentru a obține mărci de calitate de la Uniunea Europeană.
Materiale și metode
Colectarea de germoplasm, material vegetal și extracția ADN
Un set de 13 populații din rasa locală ARO au fost achiziționate în cadrul unui proiect din regiunea Apulia (BiodiverSO: https://www.biodiversitapuglia.it/), printr-o serie de misiuni desfășurate în „Acquaviva delle Fonti”, un mic oraș din Apulia din provincia Bari, Italia. Locurile de colectare ale fiecărei accesiuni au fost cartografiate prin Sistemul de Informații Geografice (GIS) și raportate în Tabel 4. În plus, două populații din rasa locală TRO și o populație din rasa locală MCO au fost incluse în studiul de față și utilizate ca referințe. Tot materialul vegetal a fost cultivat în aceleași condiții de mediu la ferma experimentală „P Martucci” a Universității din Bari (41° 1'22.08″ N, 16°54'25.95″ E), în cușcă de protecție pentru a evita polenizarea încrucișată între populaţiilor şi asigurarea polenizării intra-populaţionale prin intermediul muştelor muştenii (Lucilia caesar). Cele 16 populații au fost caracterizate pentru trăsături legate de mărimea și forma bulbului și culoarea pielii și a cărnii (Tabelul S1). În plus, analiza conținutului de solubil solid a fost efectuată utilizând un refractometru de mână și a fost măsurată picătura în probe de suc de ceapă adăugând 2,4-dinitrofenil hidrazină (0.125% v/v în 2N de HCI) și evaluând absorbanța la 420 nm, așa cum este raportat de [31]. Testul Duncan cu intervale multiple și testul SNK au fost efectuate pentru a determina prezența diferențelor semnificative.
Tabelul 4. Lista populațiilor colectate și genotipizate în acest studiu. Pentru fiecare populație, sunt raportate codul de identificare, numele local, coordonatele GPS și banca de gene care conservă semințele.
| Cod | Nume si Prenume | Coordonatele GPS | Banca de gene y |
| ARO1 | Cipolla rossa di Acquaviva | 40°54’21.708″ N 16°49’1.631” E | Di.SSPA |
| ARO2 | Cipolla rossa di Acquaviva | 40°53’14.28″ N 16°48’56.879” E | Di.SSPA |
| ARO3 | Cipolla rossa di Acquaviva | 40°54’11.304″ N 16°49’13.079” E | Di.SSPA |
| ARO4 | Cipolla rossa di Acquaviva | 40°54’3.348″ N 16°40’27.011” E | Di.SSPA |
| ARO5 | Cipolla rossa di Acquaviva | 40°51’59.76″ N 16°53’0.527” E | Di.SSPA |
| ARO6 | Cipolla rossa di Acquaviva | 40°52’48.72″ N 16°49’43.247” E | Di.SSPA |
| ARO7 | Cipolla rossa di Acquaviva | 40°53’13.47″ N 16°50’23.783” E | Di.SSPA |
| ARO8 | Cipolla rossa di Acquaviva | 40°53’18.816″ N 16°49’33.888” E | Di.SSPA |
| ARO9 | Cipolla rossa di Acquaviva | 40°54"51.372 inchi N 16°49"3.504Matei 22:21 E | Di.SSPA |
| ARO10 | Cipolla rossa di Acquaviva | 40°54’1.188″ N 16°49’24.311” E | Di.SSPA |
| ARO11 | Cipolla rossa di Acquaviva | 40°52"49.8 inchi N 16°49"48.575Matei 22:21 E | Di.SSPA |
| ARO12 | Cipolla rossa di Acquaviva | 40°52’38.892″ N 16°49’28.379” E | Di.SSPA |
| ARO13 | Cipolla rossa di Acquaviva | 40°53’21.768″ N 16°49’29.711” E | Di.SSPA |
| TRO1 | Cipolla rossa lunga di Tropea | - | Di.SSPA |
| TRO2 | Cipolla rossa tonda di Tropea | - | Di.SSPA |
| MCO | Cipolla ramata di Montoro | - | Di.SSPA |
| y Di.SSPA, Departamentul de Științe ale Solului, Plantelor și Alimentelor, Universitatea din Bari. |
Material de frunze de 20 de genotipuri per populație a fost prelevat și depozitat la -80 ° C până la utilizare. Pentru speciile bogate în polizaharide, ca A. cepa, primii pași de îndepărtare a polizaharidei sunt esențiali pentru a obține ADN de bună calitate, prin urmare spălările inițiale în tampon STE (0.25 M zaharoză, 0.03 M Tris, 0.05 M EDTA) au fost efectuate așa cum este descris de [52]. ADN-ul total a fost extras prin metoda CTAB [53] și în final a fost verificată pentru calitate și concentrație prin spectrofotometru UV-vis Nano Drop 2000 (ThermoScientific, Waltham, MA, SUA) și electroforeză cu gel de agaroză 0.8%.
Analiza SSR
16 combinații de primeri EST-SSR dezvoltate de [54] și testat anterior în studii de diversitate genetică de către [43] și [44] și 21 SSR genomic [45-unu] au fost verificați pentru a evalua caracterul adecvat al acestora (Tabelul suplimentar S4). Genotiparea a fost efectuată utilizând metoda de etichetare fluorescentă economică în care coada M13 este adăugată la fiecare primer SSR înainte [56]. Amestecuri PCR au fost preparate în reacție de 20 gL care conține: 50 ng de ADN total, 0.2 mM de amestec dNTP, 1X tampon de reacție PCR, 0.8 U de ADN polimerază DreamTaq (Thermo Scientific, Waltham, MA, SUA), 0.16 gM de primer invers , 0.032 gM de primer direct extins cu secvența M13 (5′-TGTAAAACGACGGCCAGT-3′) și 0.08 gM de primer M13 universal marcat cu coloranți fluorescenți FAM sau NED (Sigma-Aldrich, St. Louis, MO, SUA). Reacțiile PCR au fost efectuate în termociclorul SimpliAmp (Applied Biosystems, CA, SUA) cu următoarele condiții pentru majoritatea perechilor de primeri: 94 °C timp de 5 minute, 40 de cicluri la 94 °C timp de 30 s, 58 °C timp de 45 s și 72 °C timp de 45 s și o alungire finală la 72 °C timp de 5 min. În ceea ce privește ACM446 și ACM449, a fost aplicată o PCR de touchdown cu recoacere de la 60 °C la 55 °C în 10 cicluri, 30 de cicluri la 55 °C, urmată de o extensie finală de 5 minute la 72 °C. Produsele PCR au fost încărcate într-o placă cu 96 de godeuri și amestecate cu 14 gL de Hi-Di Formamidă (Life Technologies, Carlsbad, CA, SUA) și 0.5 gL GeneScan 500 ROX Size Standard (Life Technologies, Carlsbad, CA, SUA). Ampliconii au fost rezolvați cu ajutorul mașinii de secvențiere capilară ABI PRISM 3100 Avant Genetic Analyzer (Life Technologies, Carlsbad, CA, SUA), unde alelele au fost marcate ca co-dominante și atribuite utilizând software-ul GeneMapper Versiunea 3.7.
Software-urile GenAlEx 6.5 [57] și Cervus 3.0.7 [58] au fost utilizate pentru a estima numărul de alele (Na), numărul de alele efective (Ne), heterozigozitatea observată (Ho), heterozigositatea așteptată (He), conținutul de informații polimorfe (PIC), indicele de informații Shannon (I) și indicele de fixare (Fis). ) pentru fiecare locus SSR.
Evaluarea diversității genetice
Împărțirea ierarhică a variației genetice între și în cadrul populațiilor de ceapă a fost evaluată de GenAlEx 6.5 [57] prin analiza varianței moleculare (AMOVA) cu 999 bootstrapping pentru a testa semnificația. Mai mult, software-ul GenAlEx 6.5 a fost folosit pentru a estima diversitatea în cadrul fiecărei populații prin calculul mediei Ho, He și Fis pe toți loci SSR.
Structura populației a fost dedusă de algoritmul de clusterizare bazat pe model bayesian implementat în software-ul STRUCTURE v.2.3.4 [59]. Setul de date a fost rulat cu un număr de grupuri ipotetice (K), variind de la 1 la 10, stabilind zece rulări independente pentru fiecare valoare K. Pentru fiecare rulare, cu scopul de a verifica consistența rezultatelor, au fost efectuate 100,000 de perioade inițiale de ardere și 100,000 de iterații Markov Chain Monte Carlo (MCMC) sub modelul de amestec și frecvențele alelelor independente între populații. Cea mai probabilă valoare K a fost determinată prin implementarea metodei AK, descrisă de [60], în programul web STRUCTURE HARVESTER [61]. O populație individuală a fost atribuită unui grup specific atunci când coeficientul său de apartenență (valoarea q) a fost mai mare de 0.7, în caz contrar, a fost considerată de origine mixtă.
Analiza coordonatelor principale a fost efectuată pentru a vizualiza modelele de relație genetică între accesări relevate de matricea distanței genetice a lui Nei (Tabelul suplimentar S5). Pe baza frecvențelor alelelor, a fost construită o dendrogramă a distanței genetice, implementând metoda grupurilor de perechi neponderate cu medii aritmetice (UPGMA) analiza clusterului în software-ul POPTREEW. [62]. Bootstrapping a fost aplicat pentru a evalua încrederea în gruparea ierarhică, stabilind 100 de reeșantionare a setului de date. În sfârșit, software-ul MEGA X [63] a fost folosit ca software pentru desenarea arborilor.
Materiale suplimentare: Următoarele sunt disponibile online la http://www.mdpi.com/2223-7747/9/2/260/s1. Tabelul S1: Caracterizarea morfologică a bulbilor ARO, MCO și TRO. Tabelul S2: Indici de heterozigozitate și fixare calculați pentru rasele locale ARO și TRO și MCO. Tabelul S3: Valorile perechi ale parametrului Fpt. Tabelul S4: Lista SSR-urilor utilizate în studiu. Tabelul S5. Matricea populației perechi a distanței genetice Nei. Figura S1: Diagramă cu linii cu valorile K care se schimbă cu Delta K a lui Evano.
Contribuții autor: CL și LR au conceput studiul și au conceput experimentul; CL și PI au efectuat analize de markeri moleculari; ARM și VZ au efectuat testele de teren; RM, SP, GR și CL au fost implicați în analiza datelor; RM și CL au scris manuscrisul. Toți autorii au citit și au fost de acord cu versiunea publicată a manuscrisului.
Finanțarea: Această lucrare a fost finanțată de proiectul regional din Apulia „Biodiversitatea speciilor de legume din Apulia”—Programma di Sviluppo Rurale per la Puglia 2014-2020. Misura 10—Sottomisura 10.2; grant CUP H92C15000270002, Italia.
Recunoasteri: Mulțumiri se datorează „Azienda Agricola Iannone Anna” și „Associazione produttori della vera cipolla rossa di Acquaviva” pentru furnizarea de materiale vegetale utilizate în experiment.
Conflicte de interese: Autorii nu declară nici un conflict de interese.
Referinte
- 1. Stearn, WT Câte specii de Allium sunt cunoscute? Kew Mag. 1992, 9, 180-182. [CrossRef]
- 2. FAOSTAT. Baza de date statistice FAO. Disponibil online: http://www.fao.org/2017 (accesat la 8 ianuarie 2019).
- 3. Block, E. Chimia usturoiului și a cepei. Sci. A.m. 1985, 252, 114-119. [CrossRef]
- 4. Lee, B.; Jung, JH; Kim, HS Evaluarea cepei roșii asupra activității antioxidante la șobolan. Food Chim. Toxicol. 2012, 50, 3912-3919. [CrossRef]
- 5. Lee, SM; Moon, J.; Chung, JH; Cha, YJ; Shin, MJ Efectul extractelor de coajă de ceapă bogate în quercetină asupra trombozei arteriale la șobolani. Food Chim. Toxicol. 2013, 57, 99-105. [CrossRef] [PubMed]
- 6. Yoshinari, O.; Shiojima, Y.; Igarashi, K. Efectele anti-obezitate ale extractului de ceapă la șobolani grasi diabetici zucker. Nutrienți 2012, 4,1518-1526. [CrossRef]
- 7. Akash, MSH; Rehman, K.; Chen, S. Spice plant Allium cepa: Supliment alimentar pentru tratamentul diabetului zaharat de tip 2. Nutriţie 2014, 30, 1128-1137. [CrossRef] [PubMed]
- 8. Wang, Y.; Tian, WX; Ma, XF Efectele inhibitoare ale cepei (Allium cepa L.) extract de proliferare a celulelor canceroase și a adipocitelor prin inhibarea sintetazei acizilor grași. Pac asiatic. J. Cancer Prev. 2012,13, 5573-5579. [CrossRef] [PubMed]
- 9. Lai, WW; Hsu, SC; Chueh, FS; Chen, YY; Yang, JS; Lin, JP; Lien, JC; Tsai, CH; Chung, JG Quercetina inhibă migrarea și invazia celulelor canceroase orale umane SAS prin inhibarea căilor de semnalizare NF-kappaB și metaloproteinazei matriceale-2/-9. Anticancer Res. 2013, 33, 1941-1950. [PubMed]
- 10. Nicastro, HL; Ross, SA; Milner, JA Usturoiul și ceapa: proprietățile lor de prevenire a cancerului. Cancer Prev. Res. 2015, 8,181-189. [CrossRef]
- 11. Forte, L.; Torricelli, P.; Boanini, E.; Gazzano, M.; Rubini, K.; Fini, M.; Bigi, A. Proprietăți antioxidante și reparatorii osoase ale hidroxiapatitei funcționalizate cu quercetină: un studiu in vitro de co-cultură a celulelor osteoblast-osteoclaste-endoteliale. Acta Biomater. 2016, 32, 298-308. [CrossRef]
- 12. Yamazaki, Y.; Iwasaki, K.; Mikami, M.; Yagihashi, A. Distribuția a unsprezece precursori de aromă, derivați de S-Alk(en)il-L-cisteină, în șapte legume Allium. Științe alimentare Tehnol. Res. 2011, 17, 55-62. [CrossRef]
- 13. Block, E. Chimia organosulfurată a genului Allium — Implicații pentru chimia organică a sulfului. Angew. Chim. Int. Ed. Engl. 1992, 31, 1135-1178. [CrossRef]
- 14. Griffiths, G.; Trueman, L.; Crowther, T.; Thomas, B.; Smith, B. Ceapa-Un beneficiu global pentru sănătate. Phytother. Res. 2002,16, 603-615. [CrossRef]
- 15. Schwimmer, S.; Weston, WJ Dezvoltarea enzimatică a acidului piruvic în ceapă ca măsură a picantității. J. Agric. Food Chim. 1961, 9, 301-304. [CrossRef]
- 16. Ketter, CAT; Randle, WM Evaluarea picăturii în ceapă. În Studii testate pentru predare în laborator; Karcher, SJ, Ed.; Association for Biology Laboratory Education (ABLE): New York, NY, SUA, 1998; Volumul 19, p. 177-196.
- 17. Hanelt, P Taxonomie, evoluție și istorie. În Ceapa și culturile conexe, voi. I. Botanica, Fiziologie si Genetica; Rabinowitch, HD, Brewster, JL, Eds.; CRC Press: Boca Raton, FL, SUA, 1990; pp. 1-26.
- 18. Rabinowitch, HD; Currah, L. Allium Crop Science: Progrese recente; Editura CABI: Wallingford, Marea Britanie, 2002.
- 19. Mallor, C.; Carravedo, M.; Estopanan, G.; Mallor, F. Caracterizarea resurselor genetice ale cepei (Allium cepa L.) din spaniol centru secundar de diversitate. Span. J. Agric. Res. 2011, 9, 144-155. [CrossRef]
- 20. Ferioli, F.; D'Antuono, LF Evaluarea substanțelor fenolice și a sulfoxizilor de cisteină în germoplasma locală de ceapă și eșalotă din Italia și Ucraina. Genet. Resursă. Crop Evol. 2016, 63, 601-614. [CrossRef]
- 21. Petropoulos, SA; Fernandes, A.; Barros, L.; Ferreira, ICFR; Ntatsi, G. Descrierea morfologică, nutrițională și chimică a „vatikiotiko”, o specie locală de ceapă din Grecia. Food Chim. 2015,182, 156-163. [CrossRef]
- 22. Liguori, L.; Adiletta, G.; Nazzaro, F.; Fratianni, F.; Di Matteo, M.; Albanese, D. Proprietăți biochimice, antioxidante și activitate antimicrobiană a diferitelor soiuri de ceapă din zona mediteraneană. J. Food Meas. Caracter. 2019,13, 1232-1241. [CrossRef]
- 23. Yoo, KS; Pike, L.; Crosby, K.; Jones, R.; Leskovar, D. Diferențele de picătură a cepei din cauza soiurilor, mediului de creștere și dimensiunilor bulbilor. Sci. Hortic. 2006,110, 144-149. [CrossRef]
- 24. Beesk, N.; Perner, H.; Schwarz, D.; George, E.; Kroh, LW; Rohn, S. Distribuția quercetinei-3, 4′-O-diglucozidei, quercetin-4′-O-monoglucozidei și quercetinei în diferite părți ale bulbului de ceapă (Allium cepa L.) influențată de genotip. Food Chim. 2010,122, 566-571. [CrossRef]
- 25. Caruso, G.; Conti, S.; Villari, G.; Borrelli, C.; Melchionna, G.; Minutolo, M.; Russo, G.; Amalfitano, C. Efectele timpului de transplantare și densității plantelor asupra randamentului, calității și conținutului de antioxidanți al cepei (Allium cepa L.) în sudul Italiei. Sci. Hortic. 2014,166, 111-120. [CrossRef]
- 26. Perez-Gregorio, MR; Regueiro, J.; Simal-Gandara, J.; Rodrigues, AS; Almeida, DPF Creșterea valorii adăugate a cepei ca sursă de flavonoide antioxidante: o revizuire critică. Crit. Rev. Food Sci. Nutr. 2014, 54,1050-1062. [CrossRef] [PubMed]
- 27. Pohnl, T.; Schweigert, RM; Carle, R. Impactul metodei de cultivare și selecției soiurilor asupra carbohidraților solubili și principiilor înțepătoare la ceapă (Allium cepa L.). J. Agric. Food Chim. 2018, 66, 12827-12835. [CrossRef] [PubMed]
- 28. Tedesco, I.; Carbone, V.; Spagnuolo, C.; Minasi, P.; Russo, GL Identificarea și cuantificarea flavonoidelor din două soiuri din sudul Italiei Allium cepa L., Tropea (ceapa rosie) si Montoro (ceapa de cupru) si capacitatea lor de a proteja eritrocitele umane de stresul oxidativ. J. Agric. Food Chim. 2015, 63, 5229-5238. [CrossRef]
- 29. Villano, C.; Esposito, S.; Carucci, F.; Frusciante, L.; Carputo, D.; Aversano, R. Genotiparea cu randament ridicat în ceapă dezvăluie structura diversității genetice și SNP-uri informative utile pentru reproducerea moleculară. Mol. Rasă. 2019, 39, 5. [CrossRef]
- 30. Mercati, F.; Longo, C.; Poma, D.; Araniti, F.; Lupini, A.; Mammano, MM; Fiore, MC; Abenavoli, MR; Sunseri, F Variația genetică a unei roșii italiene cu termen lung de valabilitate (Solanum lycopersicum L.) colectare prin utilizarea SSR și trăsăturile morfologice ale fructelor. Genet. Resursă. Crop Evol. 2014, 62, 721-732. [CrossRef]
- 31. Gonzalez-Perez, S.; Mallor, C.; Garces-Claver, A.; Merino, F.; Taboada, A.; Rivera, A.; Pomar, F.; Perovic, D.; Silvar, C. Explorarea diversității genetice și a trăsăturilor de calitate într-o colecție de ceapă (Allium cepa L.) rasele locale din nord-vestul Spaniei. Genetica 2015, 47, 885-900. [CrossRef]
- 32. Lotti, C.; Iovieno, P.; Centomani, I.; Marcotrigiano, AR; Fanelli, V.; Mimiola, G.; Summo, C.; Pavan, S.; Ricciardi, L. Caracterizarea genetică, bio-agronomică și nutrițională a kale (Brassica oleracea L. var. acefală) diversitate în Apulia, sudul Italiei. Diversitate 2018,10, 25. [CrossRef]
- 33. Bardaro, N.; Marcotrigiano, AR; Bracuto, V.; Mazzeo, R.; Ricciardi, F.; Lotti, C.; Pavan, S.; Ricciardi, L. Analiza genetică a rezistenței la Orobanche crenata (Forsk.) într-un bob de mazăre (Pisum sativum L.) linie cu strigolactonă scăzută. J. Plant Pathol. 2016, 98, 671-675.
- 34. Wako, T.; Tsukazaki, H.; Yaguchi, S.; Yamashita, K.; Ito, S.; Shigyo, M. Cartografierea loci de trăsături cantitative pentru timpul de înșurubare la ceapa de mănunchi (Allium fistulosum L.). Euphytica 2016, 209, 537-546. [CrossRef]
- 35. Dhaka, N.; Mukhopadhyay, A.; Paritosh, K.; Gupta, V.; Pental, D.; Pradhan, AK Identificarea SSR-urilor genice și construirea unei hărți de legătură bazate pe SSR în Brassica juncea. Euphytica 2017, 213, 15. [CrossRef]
- 36. Anandhan, S.; Mote, SR; Gopal, J. Evaluarea identității varietale de ceapă folosind markeri SSR. Seed Sci. Tehnol. 2014, 42, 279-285. [CrossRef]
- 37. Mitrova, K.; Svoboda, P.; Ovesna, J. Selectarea și validarea unui set de markeri pentru diferențierea soiurilor de ceapă din Republica Cehă. ceh J. Genet. Rasa de plante. 2015, 51, 62-67. [CrossRef]
- 38. Di Rienzo, V.; Miazzi, MM; Fanelli, V.; Sabetta, W.; Montemurro, C. Conservarea și caracterizarea biodiversității germoplasmei de măsline din Apulia. Acta Hortic. 2018,1199,1-6. [CrossRef]
- 39. Mallor, C.; Arnedo-Andres, A.; Garces-Claver, A. Evaluarea diversității genetice a spaniolei Allium cepa rase locale pentru creșterea cepei folosind markeri microsateliți. Sci. Hortic. 2014,170, 24-31. [CrossRef]
- 40. Rivera, A.; Mallor, C.; Garces-Claver, A.; Garcia-Ulloa, A.; Pomar, F.; Silvar, C. Evaluarea diversității genetice la ceapă (Allium cepa L.) rasele locale din nord-vestul Spaniei și comparație cu variabilitatea europeană. NZJ Crop Hortic. 2016, 44, 103-120. [CrossRef]
- 41. De Giovanni, C.; Pavan, S.; Taranto, F.; Di Rienzo, V.; Miazzi, MM; Marcotrigiano, AR; Mangini, G.; Montemurro, C.; Ricciardi, L.; Lotti, C. Variația genetică a unei colecții globale de germoplasmă de năut (Cicer arietinum L.) inclusiv accesările italiene cu risc de eroziune genetică. Physiol. Mol. Biol. Plante 2017, 23, 197-205. [CrossRef]
- 42. Mazzeo, R.; Morgese, A.; Sonnante, G.; Zuluaga, DL; Pavan, S.; Ricciardi, L.; Lotti, C. Genetic diversity in broccoli rabe (Brassica rapa L. subsp. sylvestris (L.) Janch.) din sudul Italiei. Sci. Hortic. 2019, 253, 140-146. [CrossRef]
- 43. Jakse, M.; Martin, W.; McCallum, J.; Havey, M. Polimorfisme cu un singur nucleotide, indeluri și repetări simple de secvență pentru identificarea soiului de ceapă. J. Am. Soc. Hortic. Sci. 2005,130, 912-917. [CrossRef]
- 44. McCallum, J.; Thomson, S.; Pither-Joyce, M.; Kenel, F. Analiza diversității genetice și dezvoltarea markerului de polimorfism cu un singur nucleotide în ceapa bulbului cultivată pe baza markerilor de repetare a secvenței simple a etichetei de secvență exprimată. J. Am. Soc. Hortic. Sci. 2008,133, 810-818. [CrossRef]
- 45. Baldwin, S.; Pither-Joyce, M.; Wright, K.; Chen, L.; McCallum, J. Dezvoltarea unor markeri de repetare a secvenței simple genomice robuste pentru estimarea diversității genetice în interiorul și printre ceapa bulbului (Allium cepa L.) populaţii. Mol. Rasă. 2012, 30, 1401-1411. [CrossRef]
- 46. DeWoody, JA; Honeycutt, RL; Skow, LC Marcatori microsateliți în cerb cu coadă albă. J. Hered. 1995, 86, 317-319. [CrossRef] [PubMed]
- 47. Khodadadi, M.; Hassanpanah, D. ceapa iraniană (Allium cepa L.) răspunsurile soiurilor la depresia de consangvinizare. Aplicația mondială. Sci. J. 2010,11, 426-428.
- 48. Abdou, R.; Bakasso, Y.; Saadou, M.; Baudoin, JP; Hardy, OJ Diversitatea genetică a cepei de Niger (Allium cepa L.) evaluată prin markeri de repetare a secvenței simple (SSR). Acta Hortic. 2016,1143, 77-90. [CrossRef]
- 49. Pavan, S.; Lotti, C.; Marcotrigiano, AR; Mazzeo, R.; Bardaro, N.; Bracuto, V.; Ricciardi, F.; Taranto, F.; D'Agostino, N.; Schiavulli, A.; et al. Un grup genetic distinct în năut cultivat, așa cum a fost dezvăluit de descoperirea și genotiparea markerilor la nivelul întregului genom. Genomul plantelor 2017, 2017,10. [CrossRef]
- 50. Pavan, S.; Marcotrigiano, AR; Ciani, E.; Mazzeo, R.; Zonno, V.; Ruggieri, V.; Lotti, C.; Ricciardi, L. Genotiparea prin secvențierea unui pepene galben (Cucumis melo L.) colecția de germoplasmă dintr-un centru secundar de diversitate evidențiază modelele de variație genetică și caracteristicile genomice ale diferitelor pool-uri de gene. BMC Genom. 2017, 18, 59. [CrossRef]
- 51. Di Rienzo, V.; Sion, S.; Taranto, F.; D'Agostino, N.; Montemurro, C.; Fanelli, V.; Sabetta, W.; Boucheffa, S.; Tamendjari, A.; Pasqualone, A.; et al. Fluxul genetic în rândul populației de măslini din bazinul mediteranean. Peer J. 2018, 6. [CrossRef]
- 52. Ciobanesc, LD; McLay, TG Două protocoale la scară micro pentru izolarea ADN-ului din țesutul vegetal bogat în polizaharide. J. Plant Res. 2011,124, 311-314. [CrossRef]
- 53. Doyle, JJ; Doyle, JL Izolarea ADN-ului plantelor din țesut proaspăt. Concentra 1990,12, 13-14.
- 54. Kuhl, JC; Cheung, F.; Qiaoping, Y.; Martin, W.; Zewdie, Y.; McCallum, J.; Catanach, A.; Rutherford, P.; Chiuvetă, KC; Jenderek, M.; et al. Un set unic de 11,008 etichete de secvență exprimată de ceapă dezvăluie secvența exprimată și diferențele genomice între ordinele monocotiledonee asparagales și poales. Celula plantei 2004,16, 114-125. [CrossRef]
- 55. Kim, HJ; Lee, HR; Hyun, JY; Song, KH; Kim, KH; Kim, JE; Hur, CG; Harn, CH Dezvoltarea markerului pentru testarea purității genetice a cepei folosind SSR Finder. Coreeană J. Rasa. Sci. 2012, 44, 421-432. [CrossRef]
- 56. Schuelke, M. O metodă economică pentru marcarea fluorescentă a fragmentelor PCR. Nat. Biotehnologie. 2000, 18, 233-234. [CrossRef] [PubMed]
- 57. Peakall, R.; Smouse, PE GenAlEx 6.5: Analiză genetică în Excel. Software-ul genetic al populației pentru predare și cercetare: o actualizare. bioinformatica 2012, 28, 2537-2539. [CrossRef] [PubMed]
- 58. Kalinowski, ST; Taper, ML; Marshall, TC Revizuirea modului în care programul de calculator CERVUS găzduiește eroarea de genotipizare crește succesul în atribuirea de paternitate. Mol. Ecol. 2007,16, 1099-1106. [CrossRef]
- 59. Pritchard, JK; Stephens, M.; Rosenberg, NA; Donnelly, P. Asociația de cartografiere în populații structurate. A.m. J. Hum. Genet. 2000, 67, 170-181. [CrossRef]
- 60. Evano, G.; Regnaut, S.; Goudet, J. Detectarea numărului de grupuri de indivizi folosind software-ul STRUCTURE: A simulation study. Mol. Ecol. 2005,14, 2611-2620. [CrossRef]
- 61. Earl, D.; VonHoldt, B. STRUCTURE HARVESTER: Un site web și un program pentru vizualizarea rezultatelor STRUCTURE și implementarea metodei Evano. Conserv. Genet. Resursă. 2011, 4. [CrossRef]
- 62. Takezaki, N.; Nei, M.; Tamura, K. POPTREEW: Versiunea web a lui POPTREE pentru construirea arborilor populației din datele frecvenței alelelor și calcularea altor cantități. Mol. Biol. Evol. 2014, 31, 1622-1624. [CrossRef]
- 63. Kumar, S.; Stecher, G.; Li, M.; Knyaz, C.; Tamura, K. MEGA X. Analiza genetică evolutivă moleculară pe platforme de calcul. Mol. Biol. Evol. 2018, 35, 1547-1549. [CrossRef]